Benzylalkohol
| Benzylalkohol | |
|---|---|
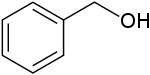 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | fenylmethanol |
| Ostatní názvy | fenylmethylalkohol, E 1519 |
| Sumární vzorec | C7H8O |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 100-51-6 |
| PubChem | 244 |
| SMILES | c1ccc(cc1)CO |
| InChI | InChI=1/C7H8O/c8-6-7-4-2-1-3-5-7/h1-5,8H,6H2 |
| Vlastnosti | |
| Molární hmotnost | 108,14 g/mol |
| Teplota tání | −15,2 °C (258,0 K) |
| Teplota varu | 205,3 °C (478,4 K) |
| Hustota | 1,044 g/cm3 |
| Index lomu | 1,5396 |
| Disociační konstanta pKa | 15,40 |
| Rozpustnost ve vodě | 3,50 g/100 ml (20 °C) 4,29 g/100 ml (25 °C) |
| Rozpustnost v polárních rozpouštědlech | rozpustný v methanolu, ethanolu a acetonu |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v diethyletheru, chloroformu a benzenu |
| Tlak páry | 180 Pa (60 °C) |
| Měrná magnetická susceptibilita | −6,64×105 μm3/g |
| Struktura | |
| Dipólový moment | 1,67 D |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −352 kJ/mol |
| Bezpečnost | |
 GHS07 Varování[1] | |
| Teplota vzplanutí | 93 °C (366 K) |
| Teplota vznícení | 436 °C (709 K) |
| Meze výbušnosti | 1,3 až 13 % |
Některá data mohou pocházet z datové položky. | |
Benzylalkohol je organická sloučenina se vzorcem C6H5CH2OH. Jedná se o bezbarvou kapalinu se slabou aromatickou vůní. Tato látka se často používá jako rozpouštědlo, a to díky své polaritě, nízké toxicitě a nízkému tlaku syté páry. Benzylalkohol se slabě rozpouští ve vodě (kolem 4 g/100 ml) a mísí se s alkoholy a diethyletherem. Anion vzniklý deprotonací alkoholové skupiny benzylalkoholu se nazývá benzylát nebo benzyloxid.
Výskyt
Benzylalkohol se přirozeně vytváří v mnoha rostlinách a často se vyskytuje v ovoci. Rovněž je obsažen v silicích mnoha rostlin, jako jsou například jasmín, hyacint a ylang-ylang. Obsahuje jej též kastoreum.[2]
Výroba
Benzylalkohol se vyrábí hydrolýzou benzylchloridu za přítomnosti hydroxidu sodného:
- C6H5CH2Cl + NaOH → C6H5CH2OH + NaCl
Také se dá získat reakcí fenylmagnesiumbromidu s formaldehydem.
Reakce
Benzylalkohol, podobně jako většina alkoholů, reaguje s karboxylovými kyselinami za vzniku esterů. V organické syntéze se benzylestery často používají jako chránicí skupiny, které lze odstranit mírnou hydrogenolýzou.[3]
Benzylalkohol reaguje s akrylonitrilem za tvorby N-benzylakrylamidu:[4]
- C6H5CH2OH + NCCHCH2 → C6H5CH2N(H)C(O)CHCH2
Použití
Benzylalkohol je častým rozpouštědlem inkoustů, vosků, barev, laků a epoxidových pryskyřic a bývá tak součástí směsí na odstraňování nátěrů, obzvláště ve směsi s látkami zvyšujícími viskozitu, které usnadňují přichycení k natřenému povrchu.[5]
Také se používá jako prekurzor řady esterů, využívaných například při výrobě mýdel a parfémů. Často bývá součástí náplní elektronických cigaret, kde navyšuje obsah vůní. Při styku 10% benzylalkoholu s poškozenou kůží nebo sliznicí funguje jako lokální anestetikum a antimikrobiální látka. Slouží také jako odmašťovací přísada v prostředcích na čištění koberců. Jakožto rozpouštědlo barev benzylalkohol usnadňuje barvení vlny, nylonu a kůže.[6] Může být také součástí repelentů.
V nanotechnologiích
Benzylalkohol se používá jako dielektrické rozpouštědlo při dielektroforetické rekonfiguraci nanovláken.[7][8]
Ve zdravotnictví
Benzylalkohol může být při nízkých koncentracích použit jako bakteriostatický konzervant u nitrožilních a povrchových léků a také v kosmetice; zabraňuje zavírání průduchů u vší, které se tak ucpou vodou nebo olejem a vši se tak udusí. Obvyklá koncentrace je 5 %.
Ostatní použití
Benzylalkohol má téměř stejný index lomu jako křemen a vlna; pokud se předmět z čistého křemene ponoří do benzylalkoholu, stane se téměř neviditelným, což lze využít k ověření, zda je tvořen skutečným křemenem. Obdobně vlna ponořená do benzylalkoholu také téměř přestane být viditelná, čímž je možné odhalit nečistoty jako jsou rostlinné materiály.
Bezpečnost
Benzylalkohol má nízkou akutní toxicitu, smrtelná dávka u krys je přibližně 1,2 g/kg[9] Rychle se oxiduje na kyselinu benzoovou, která v játrech reaguje s glycinem a vylučuje se jako kyselina hippurová. Vysoké koncentrace mohou vést k toxickým účinkům, kterými jsou selhání dechu, vazodilatace, nízký krevní tlak, křeče a ochrnutí.
Benzylalkohol silně dráždí oči,[9] v čisté podobě způsobuje odumírání rohovky.[10]
Benzylalkohol není považován za karcinogen a nejsou u něj potvrzené ani teratogenní účinky nebo reprodukční toxicita.[9]
Reference
V tomto článku byl použit překlad textu z článku Benzyl alcohol na anglické Wikipedii.
- ↑ a b Benzyl alcohol. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ Dietland Muller-Schwarze. The Beaver: Its Life and Impact. [s.l.]: [s.n.], 2003. Dostupné online. S. 43.
- ↑ FURUTA, Kyoji; GAO, Qing-Zhi; YAMAMOTO, Hisashi. Chiral (Acyloxy)borane Complex-Catalyzed Asymmetric Diels-Alder Reaction: (1R)-1,3,4-Trimethyl-3-Cyclohexene-1-Carboxaldehyde. Org. Synth.. 1995, s. 86. Dostupné online. Je zde použita šablona
{{Citation}}označená jako k „pouze dočasnému použití“.; Coll. Vol.. S. 722. Je zde použita šablona{{Citation}}označená jako k „pouze dočasnému použití“.Je zde použita šablona{{OrgSynth}}označená jako k „pouze dočasnému použití“. - ↑ PARRIS, Chester L. N-benzylacrylamide. Org. Synth.. 1962, s. 16. Dostupné online. Je zde použita šablona
{{Citation}}označená jako k „pouze dočasnému použití“.; Coll. Vol.. S. 73. Je zde použita šablona{{Citation}}označená jako k „pouze dočasnému použití“.Je zde použita šablona{{OrgSynth}}označená jako k „pouze dočasnému použití“. - ↑ Benzyl alcohol [online]. chemicalland21.com [cit. 2019-05-14]. Dostupné v archivu pořízeném dne 2009-04-21.
- ↑ Michael Ash; Irene Ash. Handbook of Preservatives. [s.l.]: Synapse Info Resources, 2004. Dostupné online. ISBN 978-1-890595-66-1. S. 292.
- ↑ Alex Wissner-Gross. Dielectrophoretic reconfiguration of nanowire interconnects. Nanotechnology. 2006, s. 4986–4990. Dostupné online. [nedostupný zdroj]
- ↑ Nanowires get reconfigured [online]. Nanotechweb.org, 19.10. 2006 [cit. 2019-05-15]. Dostupné v archivu pořízeném dne 2010-10-28.
- ↑ a b c Friedrich Brühne; Elaine Wright. Ullmann's Encyclopedia of Industrial Chemistry. [s.l.]: John Wiley & Sons, 2007. S. 7–8.
- ↑ Swarupa G. Kulkarni; Harihara M. Mehendale. Encyclopedia of Toxicology. 2. vyd. [s.l.]: Elsevier, 2005. S. 262–264.
Externí odkazy
 Obrázky, zvuky či videa k tématu benzyl alkohol na Wikimedia Commons
Obrázky, zvuky či videa k tématu benzyl alkohol na Wikimedia Commons
| Alkoholy: Alkanoly (alkoholy odvozené od alkanů) | |
|---|---|
| nižší alkanoly | methanol CH3OH • ethanol C2H5OH • propanol (propan-1-ol C3H7OH, isopropylalkohol (CH3)2CHOH) butanol (butan-1-ol, butan-2-ol, isobutanol (2-methylpropan-1-ol), 2-methylpropan-2-ol C4H9OH) • pentanol, isopentylalkohol, 2-methylbutan-1-ol, 2-methylbutan-2-ol, pentan-2-ol, pentan-3-ol, C5H11OH • hexanol C6H13OH • heptanol C7H15OH |
| mastné alkanoly | oktanol C8H17OH (oktan-1-ol, oktan-2-ol, 2-ethylhexanol) • nonanol C9H19OH • dekanol C10H21OH • undekanol C11H23OH • dodekanol C12H25OH • tridekanol C13H27OH • tetradekanol C14H29OH • pentadekanol C15H31OH • hexadekanol (cetylalkohol) C16H33OH • heptadekanol C17H35OH • oktadekanol C18H37OH • nonadekanol C19H39OH • ikosanol C20H41OH • henkosanol C21H43OH • dokosanol C22H45OH • trikosanol C23H47OH • tetrakosanol C24H49OH • pentakosanol C25H51OH • hexakosanol C26H53OH • heptakosanol C27H55OH • oktakosanol C28H57OH • nonakosanol C29H59OH • triakontanol C30H61OH |
| fenylalkanoly | benzylalkohol C6H5CH2OH • fenethylalkohol C6H5CH2CH2OH |
| alkandioly | ethandiol (ethylenglykol) C2H4(OH)2 • propan-1,2-diol (propylenglykol) C3H6(OH)2 • propan-1,3-diol C3H6(OH)2 • pentan-1,5-diol HOCH2(CH2)3CH2OH |
| alkantrioly | propantriol (glycerol) C3H5(OH)3 |










