Blaiseova reakce
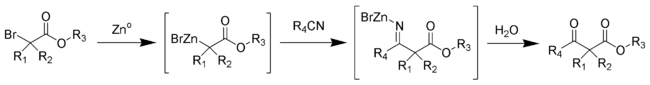
Blaiseova reakce je organická reakce, při které vzniká β-ketoester reakcí kovového zinku s α-bromesterem a nitrilem.[1]Je zde použita šablona {{Ref}} označená jako k „pouze dočasnému použití“.[2]Je zde použita šablona {{Ref}} označená jako k „pouze dočasnému použití“.[3]Je zde použita šablona {{Ref}} označená jako k „pouze dočasnému použití“. Posledním meziproduktem je metaloimin, jenž se nakonec hydrolyzuje na β-ketoester.[4]Je zde použita šablona {{Ref}} označená jako k „pouze dočasnému použití“.
Objevil ji Edmond Blaise (1872–1939) v roce 1901.
Alifatické estery s objemnými substituenty dávají při této reakci vysoké výtěžnosti. Steven Hannick a Jošito Kiši vyvinuli upravenou variantu.[5]Je zde použita šablona {{Ref}} označená jako k „pouze dočasnému použití“.
Bylo zjištěno,[6]Je zde použita šablona {{Ref}} označená jako k „pouze dočasnému použití“.[7]Je zde použita šablona {{Ref}} označená jako k „pouze dočasnému použití“. že v reakční směsi mohou být přítomny volné hydroxylové skupiny, což je u reakcí organokovových halogenidů neobvyklé.
Mechanismus
Blaiseova reakce začíná tvorbou organozinkového komplexu s bromem v poloze alfa vůči karbonylové skupině esteru. Tímto se alfa uhlík stane nukleofilním, což umožní atak elektrofilního uhlíku nitrilu. Atom dusíku v molekule nitrilu tímto získá záporný náboj a vytvoří komplex se zinkomonobromidovým kationtem. Po přidání 50% vodného roztoku uhličitanu draselného vznikne β-enaminoester (tautomer výše znázorněného iminového meziproduktu). β-ketoester lze získat jeho hydrolýzou 1M kyselinou chlorovodíkovou, která přemění enamin na keton, čímž se vytvoří β-ketoester.

Odkazy
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu Blaiseova reakce na Wikimedia Commons
Obrázky, zvuky či videa k tématu Blaiseova reakce na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku Blaise reaction na anglické Wikipedii.
- ^Je zde použita šablona
{{Note}}označená jako k „pouze dočasnému použití“. Edmond E. Blaise; Comptes rendus de l'Académie des Sciences 1901, 132, 478. - ^Je zde použita šablona
{{Note}}označená jako k „pouze dočasnému použití“. Rinehart, K. L., Jr. Organic Syntheses, Coll. Vol. 4, p. 120 (1963); Vol. 35, p. 15 (1955). (Article) - ^Je zde použita šablona
{{Note}}označená jako k „pouze dočasnému použití“. Rao, H. S. P.; Rafi, S.; Padmavathy, K. Tetrahedron 2008, 64, 8037-8043. (Review) - ^Je zde použita šablona
{{Note}}označená jako k „pouze dočasnému použití“. Cason, J.; Rinehart, K. L., Jr.; Thorston, S. D., Jr. The Journal of Organic Chemistry 1953, 18, 1594. (DOI:10.1021/jo50017a022Je zde použita šablona{{DOI}}označená jako k „pouze dočasnému použití“.) - ^Je zde použita šablona
{{Note}}označená jako k „pouze dočasnému použití“. Hannick, S. M.; Kishi, Y. The Journal of Organic Chemistry 1983, 48, 3833. (DOI:10.1021/jo00169a053Je zde použita šablona{{DOI}}označená jako k „pouze dočasnému použití“.) - [8]Je zde použita šablona
{{Ref}}označená jako k „pouze dočasnému použití“. Marko, I.E. Journal of the American Chemical Society 2007, ASAP DOI:10.1021/ja0691728Je zde použita šablona{{DOI}}označená jako k „pouze dočasnému použití“. - [9]Je zde použita šablona
{{Ref}}označená jako k „pouze dočasnému použití“. Wang, D.; Yue, J.-M. Synlett 2005, 2077–2079.









