Ethylchloorformiaat
| Ethylchloorformiaat | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
 | |||||
Structuurformule van ethylchloorformiaat | |||||
| Algemeen | |||||
| Molecuulformule | C3H5ClO2 | ||||
| IUPAC-naam | ethylchloormethanoaat | ||||
| Molmassa | 108,5236 g/mol | ||||
| SMILES | CCOC(=O)Cl | ||||
| InChI | 1S/C3H5ClO2/c1-2-6-3(4)5/h2H2,1H3 | ||||
| CAS-nummer | 541-41-3 | ||||
| EG-nummer | 208-778-5 | ||||
| PubChem | 10928 | ||||
| Wikidata | Q288339 | ||||
| Beschrijving | Kleurloze vloeistof | ||||
| Vergelijkbaar met | methylchloorformiaat | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H225 - H302 - H314 - H330 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P210 - P260 - P280 - P284 - P305+P351+P338 - P310 | ||||
| Opslag | Gescheiden van sterk oxiderende stoffen, voeding en voedingsmiddelen. Brandveilig, koel, droog en goed gesloten opslaan. | ||||
| EG-Index-nummer | 607-020-00-4 | ||||
| VN-nummer | 1182 | ||||
| ADR-klasse | Gevarenklasse 6.1 | ||||
| LD50 (ratten) | (oraal) 240 mg/kg | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | vloeibaar | ||||
| Kleur | kleurloos | ||||
| Dichtheid | (bij 20°C) 1,14 g/cm³ | ||||
| Smeltpunt | −80,6 °C | ||||
| Kookpunt | 93–95 °C | ||||
| Vlampunt | (gesloten vat) 16 °C | ||||
| Zelfontbrandings- temperatuur | 500 °C | ||||
| Dampdruk | (bij 20°C) 5400 Pa | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Ethylchloorformiaat is een organische verbinding met als brutoformule C3H5ClO2. De stof komt voor als een heldere, kleurloze vloeistof met een scherpe geur, die hevig reageert met water.
Synthese
Ethylchloorformiaat wordt bereid uit een reactie van fosgeen en ethanol, onder afsplitsing van zoutzuur:[1]
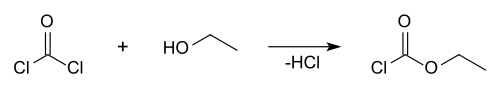
Synthese van ethylchloorformiaat.
Toepassingen
Ethylchloorformiaat dient als tussenproduct bij de bereiding van verschillende organische verbindingen, voornamelijk van carbonaten en carbamaten, die in de farmaceutische industrie als uitgangsstof voor chemische syntheses dienen.
Toxicologie en veiligheid
De stof ontleedt bij verhitting, met vorming van giftige en irriterende dampen, onder andere waterstofchloride en fosgeen. Ze reageert bij contact met water of waterdamp, waardoor giftig, corrosief waterstofchloride en ethylformiaat wordt gevormd:
Ethylchloorformiaat reageert hevig met sterk oxiderende stoffen, waardoor kans op brand en ontploffing ontstaat. De stof reageert met amines, water en basen. Ze tast vele metalen aan, in het bijzonder in aanwezigheid van water.
Ethylchloorformiaat veroorzaakt tranende ogen. Ze is corrosief voor de ogen, de huid en de luchtwegen. Inademing van de dampen kan longoedeem veroorzaken.
Externe links
 ethylchloorformiaat - International Chemical Safety Card
ethylchloorformiaat - International Chemical Safety Card
- ↑ (en) ETHYL CHLOROFORMATE, chemicalland21
















