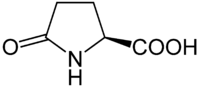
Piroglutaminska kiselina
 | |
| Nazivi | |
|---|---|
| Preferisani IUPAC naziv Pidolic acid | |
| Sistemski IUPAC naziv 5-Oksopirolidin-2-karboksilna kiselina | |
| Drugi nazivi 5-Oksoprolin 5-Okso-prolin | |
| Identifikacija | |
| |
3D model (Jmol) |
|
| 3DMet | B01549 |
| Abrevijacija | Glp |
| Bajlštajn | 82134 |
| ChEBI |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA InfoCard | 100.005.227 |
| EC broj | 205-748-3 |
| Gmelin Referenca | 1473408 |
| KEGG[1] |
|
| MeSH | Pyrrolidonecarboxylic+acid |
PubChem[2][3] C ID |
|
| RTECS | TW3710000 |
| UNII |
|
SMILES
| |
| Svojstva | |
| C5H7NO3 | |
| Molarna masa | 129,12 g·mol−1 |
| Tačka topljenja | 184 °C (363 °F; 457 K) |
| log P | -0,89 |
| Kiselost (pKa) | -1,76, 3,48, 12,76 |
| Baznost (pKb) | 15,76, 10,52, 1,24 |
| Izoelektrična tačka | 0,94 |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
 Y verifikuj (šta je Y verifikuj (šta je  Y Y Н ?) Н ?) | |
| Reference infokutije | |
Piroglutaminska kiselina (5-oksoprolin, pidolinska kiselina, piroglutamat) je uobičajeni derivat aminokiseline u kome je slobodna amino grupa glutaminske kiseline ili glutamina ciklizovana da formira laktam. Ona je prisutna u mnogim proteinima uključujući bakteriorodopsin. N-terminalna glutaminska kiselina i glutaminski ostaci se mogu spontano ciklizovati i formirati piroglutamat. Ona je jedna od nekoliko formi blokiranih N-terminala koji predstavljaju problem za N-terminalno sekvenciranje koristeći Edmanovu hemiju, za koje je neophodna slobodna primarna amino grupa. Enzim piroglutamatna aminopeptidaza može da povrati slobodni N-terminus odsecanjem piroglutamatnog ostatka.[4]
Piroglutamatna kiselna je takođe poznata kao pidolinska kiselina. Ona postoji kao dva distinktna enantiomera:
- (2R) ili (+) ili l ili D
- (2S) ili (–) ili d ili L
Reference
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003. уреди
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Podell David N., Abraham George N. (1978), „A technique for the removal of pyroglutamic acid from the amino terminus of proteins using calf liver pyroglutamate amino peptidase”, Biochem. Biophys. Res. Commun., 81 (1): 176—85, PMID 26343, doi:10.1016/0006-291X(78)91646-7 .
Spoljašnje veze
- p
- r
- u
aminokiseline
| Serin/ Treonin | |
|---|---|
| Tirozin | Fosforilacija · Sulfacija · Vezivanje za porfirinski prsten · vezivanje flavina · formiranje p-hidroksibenziliden-imidazolona · formiranje Lizin tirozil kinona (LTQ) · formiranje topakinona (TPQ) |
| Cistein | |
| Aspartat | Formiranje sukcinimida |
| Glutamat | |
| Asparagin | |
| Glutamin | |
| Lizin | Metilacija · Acetilacija · Acilacija · Hidroksilacija · Ubikvitinacija · Sumoilacija · Dezmozin · ADP-ribozilacija · Deaminacija i oksidativna deaminacija do aldehida · O-glikozilacija · formiranje Imina · Glikacija · Karbamilacija |
| Arginin | |
| Prolin | |
| Histidin | Formiranje diftamida |









