| S100A2 |
|---|
 |
| Наявні структури |
|---|
| PDB | Пошук для людей: PDBe RCSB |
|---|
| Список кодів PDB | | 2RGI, 4DUQ | | |
| Ідентифікатори |
|---|
| Символи | S100A2, CAN19, S100L, S100 calcium binding protein A2 |
|---|
| Зовнішні ІД | OMIM: 176993 HomoloGene: 48389 GeneCards: S100A2 |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • зв'язування з іоном металу
• calcium ion binding
• identical protein binding
• GO:0001948, GO:0016582 protein binding
• transition metal ion binding
|
|---|
| Клітинна компонента | • компонент клітини
|
|---|
| Біологічний процес | • endothelial cell migration
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | NM_005978
NM_001366406
NM_001366407 |
| |
|---|
| RefSeq (білок) | | NP_005969
NP_001353335
NP_001353336 |
| |
|---|
| Локус (UCSC) | н/д | н/д |
|---|
| PubMed search | [1] | н/д |
|---|
| Вікідані |
|
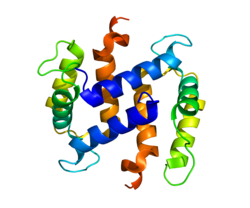
S100A2 (англ. S100 calcium binding protein A2) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 1-ї хромосоми. [2] Довжина поліпептидного ланцюга білка становить 98 амінокислот, а молекулярна маса — 11 117[3].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MMCSSLEQAL | | AVLVTTFHKY | | SCQEGDKFKL | | SKGEMKELLH | | KELPSFVGEK |
| VDEEGLKKLM | | GSLDENSDQQ | | VDFQEYAVFL | | ALITVMCNDF | | FQGCPDRP |
Білок має сайт для зв'язування з іонами металів, іоном кальцію.
Література
- Lee S.W., Tomasetto C., Swisshelm K., Keyomarsi K., Sager R. (1992). Down-regulation of a member of the S100 gene family in mammary carcinoma cells and reexpression by azadeoxycytidine treatment. Proc. Natl. Acad. Sci. U.S.A. 89: 2504—2508. PMID 1372446 DOI:10.1073/pnas.89.6.2504
- Wicki R., Franz C., Scholl F.A., Heizmann C.W., Schaefer B.W. (1997). Repression of the candidate tumor suppressor gene S100A2 in breast cancer is mediated by site-specific hypermethylation. Cell Calcium. 22: 243—254. PMID 9481475 DOI:10.1016/S0143-4160(97)90063-4
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Shimamoto S., Kubota Y., Tokumitsu H., Kobayashi R. (2010). S100 proteins regulate the interaction of Hsp90 with cyclophilin 40 and FKBP52 through their tetratricopeptide repeats. FEBS Lett. 584: 1119—1125. PMID 20188096 DOI:10.1016/j.febslet.2010.02.055
- Koch M., Diez J., Fritz G. (2008). Crystal structure of Ca2+ -free S100A2 at 1.6-A resolution. J. Mol. Biol. 378: 933—942. PMID 18394645 DOI:10.1016/j.jmb.2008.03.019
Примітки
- ↑ Human PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:10492 (англ.) . Архів оригіналу за 14 жовтня 2017. Процитовано 25 серпня 2017.
- ↑ UniProt, P29034 (англ.) . Архів оригіналу за 27 вересня 2017. Процитовано 25 серпня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|















